Estudo mostra que Coronavírus altera o RNA das células infectadas
Os cientistas da Universidade Federal de São Paulo (Unifesp) demonstraram que a infecção pelo vírus SARS-CoV-2, o causador da Covid-19, pode alterar o padrão de funcionamento dos RNAs das células. A conclusão foi tomada após uma análise de 13 conjuntos de dados obtidos ao longo de quatro estudos que analisaram o RNA viral, inclusive como […]
13 set, 2022
Os cientistas da Universidade Federal de São Paulo (Unifesp) demonstraram que a infecção pelo vírus SARS-CoV-2, o causador da Covid-19, pode alterar o padrão de funcionamento dos RNAs das células. A conclusão foi tomada após uma análise de 13 conjuntos de dados obtidos ao longo de quatro estudos que analisaram o RNA viral, inclusive como o de células animais e humanas.
No mais recente deles, publicado na revista Frontiers in Cellular and Infection Microbiology, foram analisadas modificações ou epitranscriptoma, que corresponde ao conjunto de modificações bioquímicas do RNA dentro de uma célula, nas células Vero (derivadas dos macacos) e da linhagem Calu-3 humanas utilizando uma técnica de sequenciamento direto do RNA. Por exemplo, a metilação é uma modificação bioquímica que ocorre nas células por meio da ação de enzimas capazes de transferir parte de uma molécula para outra. Isso altera o comportamento de proteínas, enzimas, hormônios e genes.
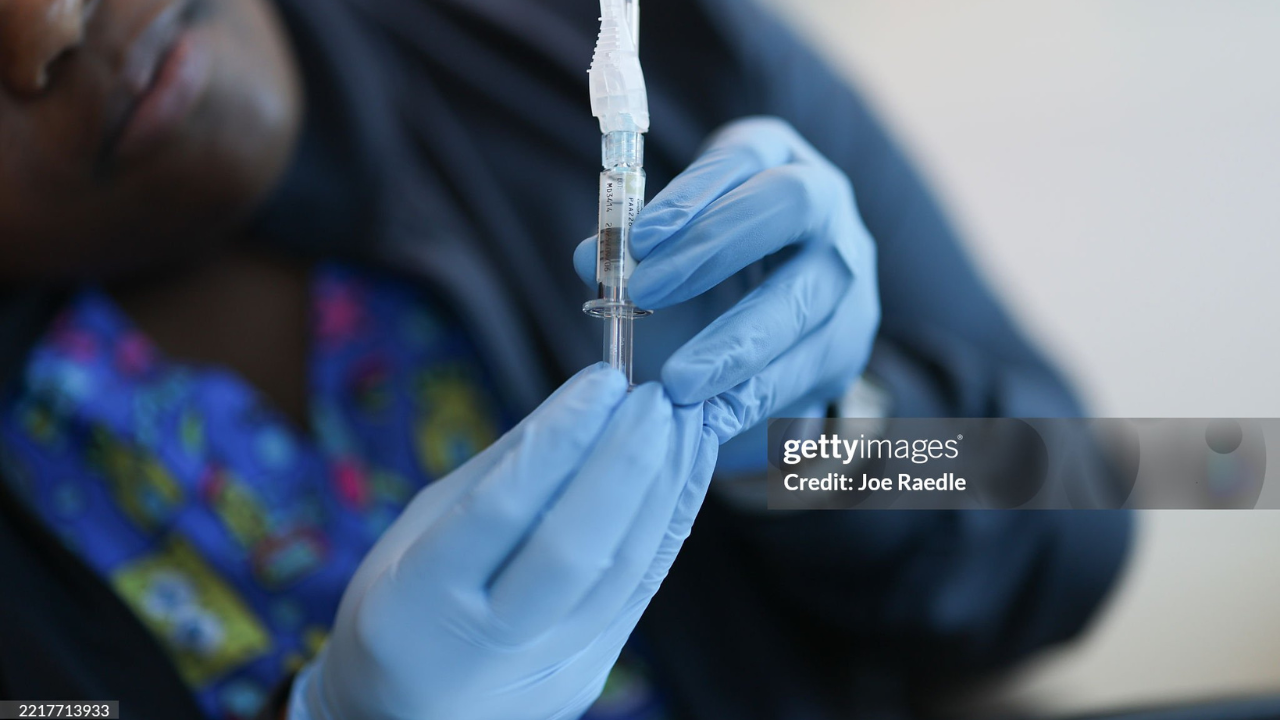
 Coronavírus (Reprodução/NEXU Science)
Coronavírus (Reprodução/NEXU Science)
Neste estudo, os pesquisadores demonstraram quantitativamente as alterações no RNA das células infectadas analisando todo o conjunto de RNA presente nas células infectadas, qualitativamente indicando individualmente o número de metilação em cada base em um mapa do RNA dessas células. “Nosso primeiro achado importante neste trabalho é que a infecção pelo SARS-CoV-2 aumenta no conjunto de RNAs da célula o nível global de metilação do tipo m6A [N6-metiladenosina], em comparação com as células não infectadas”, diz Marcelo Briones, pesquisador do Centro de Bioinformática Médica da Escola Paulista de Medicina (EPM-Unifesp) e coordenador da investigação.
O estudo é a continuação de um trabalho que foi publicado em 2021, que analisava o epigenoma do vírus demonstrando o padrão da metilação em seu RNA. “Nos vírus, a metilação tem duas funções: regular a expressão das proteínas e defender o patógeno [agente causador de doenças] da ação do interferon, uma potente substância antiviral fabricada pelo organismo hospedeiro”, diz Briones.
Nos dois trabalhos, os pesquisadores analisaram o tipo mais comum de modificação de nucleotídeo de RNA, o m6A, que está envolvido em vários processos cruciais dos RNAs, como a localização intracelular e a capacidade de produzir proteínas. Os nucleotídeos são compostos de quatro bases nitrogenadas diferentes (adenina, guanina, citosina e uracila) sendo distribuídas ao longo das fitas de RNA encontradas em cada célula.
A equipe também observou que diferentes cepas de vírus diferiam na sequência de bases nitrogenadas que compõem seus nucleotídeos. “Desse modo, algumas cepas podem ser mais bem ‘metiladas’ do que outras e, assim, proliferar melhor dentro das células”, diz Briones. Uma sequência de nucleotídeos foi observada, conhecida como “DRACH”, receptora da metilação m6A, sendo um pouco diferente nos RNAs do SARS-CoV-2 em comparação aos RNAs das células.
Nesta sigla, muito utilizada no estudo dos tipos, a letra D significa as bases nitrogenadas adenina, guanina ou uracila; a letra R significa adenina ou guanina; a letra A significa resíduos metilados; a letra C corresponde a citosina; a letra H representa adenina, citosina ou uracilo. Como o vírus usa as enzimas da célula para se metilar, isso aumenta a pressão evolutiva sobre o vírus para adaptar sua sequência “DRACH” para ser mais como uma célula.
As cepas de vírus mais capazes de realizar essa adaptação também evitarão o interferon com mais eficiência. Após concluir sua análise do papel do SARS-CoV-2 no binômio patógeno-hospedeiro em relação às modificações de m6A, o próximo passo para os cientistas será analisar os dados armazenados para rastrear a correlação entre os níveis de metilação do RNA viral e a proliferação viral Quociente – ou burst size.
“Quanto mais ‘metilado’ o vírus está, mais crescerá no citoplasma celular e maior será o seu burst size”, explica Briones. Normalmente, sem presença de estímulos, uma partícula viral pode se replicar em mil outras. “Os achados abrem a perspectiva para novos tratamentos para a Covid-19 e o reposicionamento de drogas conhecidas”, completa o pesquisador.
Além disso, ainda há elementos para a melhor compreensão da capacidade das sublinhagens em escapar ao sistema imune. Como foram feitas as análises Cientistas da Unifesp usaram uma abordagem de sequenciamento direto de RNA. Segundo os pesquisadores, uma das vantagens dessa técnica é que ela evita a modificação das fitas de RNA lidas por métodos convencionais de diagnóstico molecular (RT-PCR). Para o teste de RT-PCR, as moléculas de RNA são copiadas e convertidas em DNA complementar, ou cDNA. Nesse processo, moléculas que antes tinham nucleotídeos de fita simples agora têm duas fitas. As moléculas de cDNA são então amplificadas, gerando bilhões de clones.
Para Briones, há muitos laboratórios realizando as sequências de coronavírus a partir de cDNA, o que pode gerar alguns vieses e confundir os pesquisadores. “Alguns acham que as trocas de nucleotídeo ocorrem, na verdade, porque havia ali uma base epigeneticamente modificada. Isso precisa ser investigado e de uma maneira sistemática”, comenta.
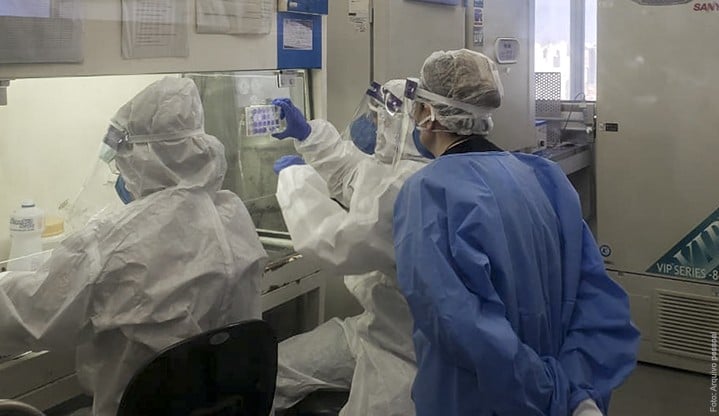
Foto destaque: Pesquisas da Unifesp e coordenado pelo docente Mario Janini (Reprodução/Unifesp)